|
|
eğitim öğretim ile ilgili belgeler > konu anlatımlı dersler > FEN BİLİMLERİ dersi ile ilgili konu anlatımlar
KARIŞIM NEDİR TANIMI KARIŞIMLARIN ÖZELLİKLERİ ÇEŞİTLERİ KARIŞIMLARIN AYRIŞTIRILMASI AYRIŞTIRMA YÖNTEMLERİ (FEN BİLİMLERİ DERSİ KONU ANLATIM)
Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir.
İki farklı maddenin kendi özelliklerini kaybetmeden bir arada bulunması ile oluşur.
Örnek: Tuzlu su. Tuz ve su kendi özelliklerini kaybetmeden bir arada bulunurlar.
Karışımların özellikleri
1. Birden fazla maddenin karışması ile oluşur.
2. Karışımı oluşturanlar kendi özelliklerini kaybetmezler.
3. Maddeler her oranda karışabilir.
4. Fiziksel yolla ayrılırlar.
5. Saf madde değildir.
6. Formül ile yazılmazlar.
7. Belirli bir erime, kaynama noktaları yoktur.
8. Homojen veya heterojen olabilir.
9. Karışımlar homojen ve heterojen olmak üzere ikiye ayrılır.

GÖRÜNÜMLERİNE GÖRE KARIŞIM ÇEŞİTLERİ 2'YE AYRILIR:
1-Heterojen Karışımlar (Adi Karışımlar): Karışımı oluşturan maddeler karışımın her tarafına eşit miktarlarda dağılmaz.

Karışımı oluşturan maddeler her tarafa eşit olarak dağılmaz. Heterojen karışımlara adi karışım da denir. Yağ-su, ayran, çamur, kum-su heterojen karışımdır.
Not: Ayran, süt ilk bakışta homojen karışım gibi görünebilir. Bir süre beklendiğinde yoğurt dibe çöker, sütün üzerinde kaymak oluşur. Bu nedenle süt ve ayran heterojen karışımlardır.
Örnek: (tebeşir tozu+ su), (zeytinyağ+su)
Süt, ayran, toprak, beton, sis vb.
a. Süspansiyon (katı- sıvı)
Bir katının sıvı içerisinde çözünmeyip, parçacıklar (asılı) halinde kalmasıyla oluşan karışımlardır.
Örnek: ayran, pişmiş Türk kahvesi, çamurlu su, tebeşirli su, hoşaf, taze sıkılmış meyve suyu, kan vb.
b. Emülsiyon (sıvı- sıvı)
Bir sıvının başka bir sıvı içerisinde çözünmeden kalmasıyla oluşan karışımlardır.
Örnek: zeytinyağı-su, benzin-su, süt vb.
c. Aerosol (sıvı- gaz)
Bir sıvının gaz ile oluşturduğu heterojen karışımlardır. Örnek: deodorantlar, sis, spreyler
Heterojen Karışımların Özellikleri:
1- Heterojen özellik gösterirler.
2- Bulanık görünürler.
3- Dipte çökelti oluştururlar.
4- Genellikle tanecikleri gözle görülür.
5- Fiziksel yolla (süzme) ayrılırlar.
2-Homojen Karışımlar (Çözeltiler): Karışımı oluşturan maddeler, karışımın her tarafına eşit olarak dağılmışlardır.

Karışımı oluşturan maddeler her tarafa eşit olarak dağılmıştır. Tuz-su, Şeker-su, alkol-su homojen karışımdır. Homojen karışımlara çözelti adı da verilmektedir.
Örnek: bronz, çelik, sirke, hava, tuzlu su vb.
Çözeltiler fiziksel hallerine bağlı olarak katı, sıvı veya gaz halde bulunabilirler.
a. Katı-Katı çözeltiler:
Alaşımlar =metal+metal
b. Sıvı çözeltiler:
Sıvı- Katı: burun damlası, şerbet
Sıvı- Sıvı: kolonya, sirke
Sıvı- Gaz: gazoz, deniz suyu
c. Gaz çözeltiler:
Gaz- gaz çözeltiler= hava, doğalgaz...
Homojen Karışımların Özellikleri
1- Homojendirler
2- Dipte çökelti oluşturmazlar.
3- Berrak görünüşlüdürler.
4- Tanecikleri gözle görülmez.
5- Süzme ile ayrılmazlar.
6- Belirli erime, kaynama noktaları yoktur. Çözünen madde miktarı arttıkça kaynama nok. yükselir, donma nok. azalır.
KARIŞIMLARIN AYRIŞTIRILMASI
Karışımlar fiziksel yollarla meydana gelmektedir. Bu nedenle fiziksel yollarla birbirinden ayrılırlar.
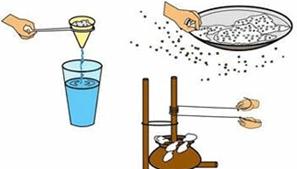
Karışımların Ayrılma Yöntemleri
1. Buharlaştırma Yöntemi
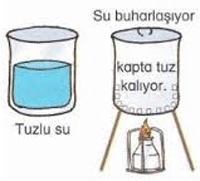
Karışımlar ısıtılarak içerisindeki sıvılar buharlaştırılır. Karışım içindeki katı madde çökerek ayrışmış olur. Tuz gölünde suyun buharlaşması sonucu tuz dibe çöker. Şeker üretilmesi, pestil yapımı buharlaştırma yöntemi ile yapılır.
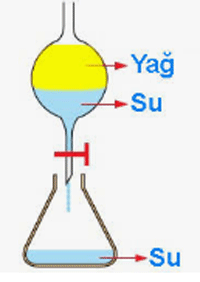
2. Yoğunluk farkı ile ayırma

Yoğunlukları farklı olan maddeler karışımların içinden ayrılabilir. Su- yağ karışımı ayırma hunisine alınır, suyun aşağıya çökmesi beklenir. Su musluktan akıtılır, bu şekilde su yağdan ayrılmış olur.
3. Damıtma ile Ayırma
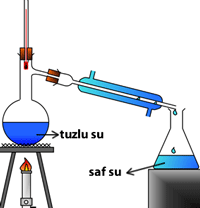
Birbiri ile karışmış olan sıvıların ayrılmasında kullanılan bir yöntemdir. Sıvıların kaynama noktaları farkı ile birbirinden ayrılır. Kaynama noktası düşük olan sıvı önce kaynayarak sıvıdan ayrılacaktır. Başka bir kapta buhar yoğunlaştırılarak sıvılar birbirinden ayrılır.
4. Mıknatısla Ayırma

Mıknatıs demir, nikel, kobalt elementlerini ve bunlardan yapılan maddeleri çekmektedir. Karışım (bilgi yelpazesi. com) içerisinde demir, nikel ve kobalt varsa mıknatısla ayırım sağlanabilir. Kum içerisinde demir tozları mıknatısla ayrılabilir.
5.Elektriklenme ile Ayırma
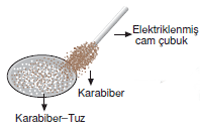
Sürtünme ile elektrik yükü kazanan plastik, cam gibi maddeler bazı maddeleri çekerler. Örneğin elektrik yüklü cam çubuk tuz karabiber karışımından karabiberleri çeker. Bu şekilde şeker-kükürt karışımından da kükürt ayrılabilir.
6. Erime Noktası Farkı ile Ayırma

Erime noktaları farklı olan iki katı karışım birbirinden bu şekilde ayrılabilir. Örneğin çink- ve kalay karışımı
7. Tanecik Boyutu Farkı ile Ayırma

Tanecikleri farklı olan maddeler bu şekilde ayrılabilir. Buna eleme yöntemi de denilmektedir. Örneğin kum ile çakıl elenerek ayrılabilir.
8. Özkütle Farkı ile Ayırma
Farklı yoğunluktaki iki maddenin ayrılmasında kullanılır. Örneğin kum ile talaş karışımını ayırmak için su içerisine atarız. Talaş suda yüzerken, kum suda batacaktır.
9. Çözünürlük Farkı ile Ayırma

İki katının ayrılmasından çözünürlüklerinden yaralanılarak ayırma yapılabilir. Bu katılardan birisi sıvıda çözünmesi diğerinin ise çözünmemesi gerekmektedir. Örneğin demir tuzu tuz karışımını su içerisine attığımızda tuz çözünürken demir tozu çözünmez. Karışım süzüldüğünde demir tozu süzgeçte kalacaktır.
ÇÖZELTİLER (HOMOJEN KARIŞIMLAR) VE ÖZELLİKLERİ

1. Çözen ve çözünen madde miktarına göre çözeltiler:
Seyreltik Çözelti: Bir başka çözeltiye göre; Çözünen madde miktarı az, çözen madde miktarı ( çözücü) fazla olan çözeltilerdir.
(Ör: 100gr su+ 1 gr şeker çözeltisi, 100gr su+ 10 gr şeker çözeltisine göre seyreltiktir.)
Derişik Çözelti: Bir başka çözeltiye göre; Çözünen madde miktarı fazla, çözücüsü az olan çözeltilerdir.
(Ör: 100gr su+ 15 gr şeker çözeltisi, 100gr su+ 5 gr şeker çözeltisine göre derişiktir.)
Seyreltik çözeltiler derişik hale getirilebilir. Bunun için:
-Çözücü (sıvı) buharlaştırılır
-Çözünen eklenir
-Çözelti soğutulur
Derişik çözeltileri seyreltik hale getirmek için;
-Çözücü eklenir.
|
|
2. Çözünebilen madde miktarına göre çözeltiler:
Doymuş Çözelti: Belli bir sıcaklıkta çözebileceği kadar çözüneni içeren çözeltilerdir.
Doymamış Çözelti: Belli bir sıcaklıkta, çözebileceğinden daha az çözünen içeren çözeltilerdir.
Aşırı Doymuş Çözelti: Çözebileceğinden daha fazla madde bulunduran çözeltilerdir.(heterojen görünürler.)
3. Elektrik akımını iletmelerine göre çözeltiler:
İletken (elektrolit) Çözeltiler: İçerisinde + ve -- yüklü iyon bulunduran çözeltiler elektrik akımını iletir. Ör: sirkeli, asitli, tuzlu, limonlu su
İletken olmayan (Elektrolit olmayan) Çözelti: İçerisinde moleküller bulunur. İyon yoktur. Bu yüzden iletken değildir. Ör: alkollü su, şekerli su, üre, kolonyalı su, saf su)
ÇÖZÜNÜRLÜK VE ÖZELLİKLERİ
Belli sıcaklıkta ve basınçta 100gr çözücü içinde çözünebilen maksimum madde miktarına çözünürlük denir. Çözünürlük, katı, sıvı, gaz maddeler için ayırt edici bir özelliktir.
Birim hacimdeki çözücüyü belli bir sıcaklıkta doyuran çözünmüş madde miktarıdır. Sulu çözeltiler için, 100cm³ Suda belli bir sıcaklıkta çözünebilen maksimum madde miktarına maksimum çözünürlük denir. t C sıcaklıkta hazırlanan Xin doymuş çözeltisi daha fazla X çözemediğine göre , X in çözünen kütlesi , o sıcaklıktaki çözünürlüğü verir. Katıların sıvılardaki çözünürlüğü bazı etkenlere bağlıdır.
Çözünme Olayı
Bir maddenin başka bir madde içerisinde gözle görülemeyecek kadar küçük taneciklere homojen olarak ayrışması olayına çözünme denilir. O halde bir madde bir (bilgi yelpazesi.net) başka madde içerisinde en küçük yapı taşına ayrışmaktadır. Bu yapıtaşları maddelerin cinsine göre, molekülleri, iyonları ve çok nadiren de atomları şeklinde olabilir.
Bu bölümde, maddelerin çözünmesi olayının yönü, çözünme miktarları ve çözünmedeki enerji davranışları incelenmektedir.
Bir katı madde, bir sıvı madde içerisine atılmış ve bir miktarı çözünmüş olsun. Bu katı maddenin sıvı içerisinde çözünmesi halinde, katıya çözünen ve sıvı maddeye de çözücü denir. Her çözünme olayında az veya çok enerji alış verişi olur. Çözünme Entalpisi adı verilen bu enerji endotermik veya ekzotermik olabilir. Bu enerji değeri bize maddenin nasıl ve ne kadar çözünebileceği hakkında bir yargı verebilir.
Çözünürlüğe Etki Eden Faktörler:
1. Basınç: Gazların çözünürlüğü basınç arttıkça artar. Basınç, katı ve sıvılarda çözünürlüğe etki etmez.
2. Sıcaklık: Katı ve sıvılarda çözünürlük, sıcaklıkla doğru orantılıdır. Gazlarda ters orantılıdır.
Örneğin Karadenizde oksijen miktarı Akdenizden daha çoktur.çünkü deniz suyu soğuktur.
3. Çözücü türü: Örneğin tuz suda çözünürken, yağda çözünmez. Şeker suda çözünürken, alkolde çözünmez.
Çözünürlük Hızına etki Eden Faktörler:
Çözünürlük hızı;
1. Sıcaklık: Sıcaklıkla doğru orantılıdır.
2. Çözünenin temas yüzeyini artırırsak artar.
3. Karıştırma, çalkalama ile doğru orantılıdır.
4. Çözünen cinsi (Tuz ve şeker su içinde farklı hızlarda çözünür.)

Element, Bileşik Ve Karışımların Karşılaştırılması
Element
Saf maddelerdir.
Kendine özgü öz kütlesi vardır.
Fiziksel veya kimyasal yöntemlerle basit maddelere ayrışmaz.
Homojendir.
Kendilerine özgü E.N, K.N vardır.
Yapıtaşı atomdur.
Aynı cins atomlardan oluşur.
Sembolle gösterilir.
Bileşik
Saf maddelerdir.
Kendine özgü öz kütlesi vardır.
Kimyasal yöntemlerle ayrışır. (elektroliz, ısıtma)
Homojendir.
Kendilerine özgü E.N, K.N vardır.
Yapıtaşı moleküldür.
Farklı cins atom, aynı cins moleküllerden oluşur.
Formüllerle gösterilir.
Elementlerin sabit oranlarda birleşmesiyle oluşur.
Elementler özelliklerini kaybeder.
Karışım
Saf değillerdir.
Sabit öz kütlesi yoktur.
Fiziksel yöntemlerle ayrışır. (süzme, eleme,damıtma)
Homojen veya heterojendir.
EN, KN belirgin değildir.
Yapıtaşı atom veya moleküldür.
Farklı cins atom ve moleküllerden oluşur.
Belli formülleri yoktur.
Karışımı oluşturan maddeler arasında belirli oran yoktur. Her oranda karışabilirler.
Karışımı oluşturan maddeler özelliklerini kaybetmezler.
|
|
>>>TIKLAYIN<<<
FEN BİLİMLERİ DERSİ İLE İLGİLİ TEST SORULARI, SORU BANKASI
SAYFASINI
GÖRMEK İSTERSENİZ
>>>TIKLAYIN<<<
FEN BİLİMLERİ DERSİ İLE İLGİLİ YAZILI SORULARI SAYFASINI GÖRMEK İSTERSENİZ
>>>TIKLAYIN<<<
| ||||